Diagramy cyklického děje 2
Úloha číslo: 415
V pV-diagramu nakreslete cyklus mezi stavy označenými 12341 skládající se ze dvou izochor (12, 34) a dvou izobar (23, 41). Předpokládejte, že platí p2 = 2p1, V3 = 4V1. Uvedený cyklus poté překreslete ještě do VT-diagramu.
Tlak a objem v počátečním stavu je označen p1, V1 a i v dalších stavech index u označení veličiny odpovídá označení stavu.
Nápověda
Pro každý děj si nejprve rozmyslete, která ze stavových veličin (p, V, T) popisujících plyn je konstantní a které jsou si sobě úměrné. Potom rozhodněte, jak daný děj zakreslit do pV a VT-diagramu.
pV-diagram
V pV-diagramu se vynáší tlak p na svislou a objem V na vodorovnou osu.
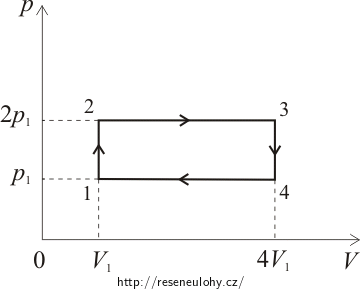
V části 12 je děj izochorický, což znamená, že se při něm nemění objem. Ději tedy odpovídá svislá úsečka začínající v bodě o souřadnicích [V1, p1] a končící v bodě o souřadnicích [V1, 2p1].
V části 23 se nemění tlak, protože se jedná o izobarický děj. Ten je v pV-diagramu znázorněn vodorovnou úsečkou končící v bodě o souřadnicích [4V1, 2p1].
Děj v části 34 je opět izochorický, a tak se po svislé úsečce dostaneme do bodu [4V1, p4].
Děj v poslední části 41 je opět izobarický, znázorňuje ho tedy vodorovná úsečka spojující body 4 a 1, a z toho také vyplývá, že musí platit p4 = p1.
Celý cyklus je, jak můžeme vidět z obrázku, v pV-diagramu znázorněn obdélníkem.
Nápověda – překreslení do VT-diagramu
Abyste mohli zakreslit uvedené děje do VT-diagramu, musíte určit, jak se při nich bude měnit teplota T plynu. K tomu využijte v případě izochorického děje tzv. Charlesův zákon a v případě izobarického děje tzv. Gay-Lussacův zákon.
VT-diagram
Ve VT-diagramu se vynáší objem V na svislou a teplota T na vodorovnou osu.
Při izochorickém ději se nemění objem. Proto bude část 12 znázorněna vodorovnou úsečkou. Zbývá zjistit, jaká teplota bude odpovídat bodu 2. K tomu využijeme tzv. Charlesův zákon ve tvaru
\[\frac{p_1}{T_1}=\frac{p_2}{T_2}.\]Z něj vyjádříme teplotu T2
\[T_2=\frac{p_2T_1}{p_1}\]a po dosazení p2 = 2p1 ihned dostáváme, že T2 = 2T1. Teplota se tedy v průběhu tohoto děje zdvojnásobí a bod 2 má souřadnice [2T1; V1].
V části 23 probíhá izobarický děj, pro který platí tzv. Gay-Lussacův zákon ve tvaru
\[\frac{V_2}{T_2}=\frac{V_3}{T_3},\]tj. objem je úměrný teplotě a izobarický děj bude ve VT-diagramu znázorněn úsečkou. Ze zadání víme, že V3 = 4V2 = 4V1. Když tento údaj dosadíme do uvedeného vzorce, zjistíme odpovídající změnu teploty:
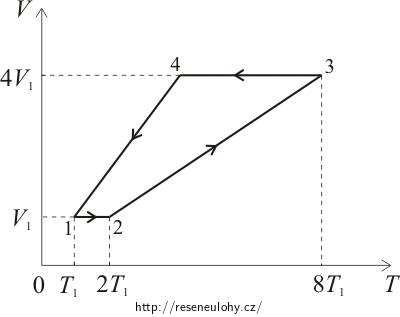
\[T_3=\frac{V_3T_2}{V_2}=4T_2=8T_1.\]Zakreslíme-li bod 3 o souřadnicích [8T1; 4V1] do diagramu, zjistíme, že je izobarický děj znázorněn úsečkou ležící na přímce procházející počátkem. To odpovídá tomu, že při izobarickém ději je objem přímo úměrný teplotě.
Následující izochorický děj 34 bude opět znázorněn vodorovnou úsečkou, protože je při něm objem konstantní. K určení toho, jak se změní teplota, použijeme Charlesův zákon ve tvaru
\[\frac{p_3}{T_3}=\frac{p_4}{T_4}.\]Z předchozí části úlohy víme, že platí
\[p_4=\frac{1}{4}p_3,\]tj. tlak v průběhu děje klesá. Po dosazení do Charlesova zákona okamžitě zjistíme, že klesne i teplota:
\[T_4=\frac{1}{2}T_3=4T_1.\]Dostali jsme se tedy do bodu 4 se souřadnicemi [4T1, 4V1].
Děj v části 41 je opět izobarický. Tlak se při něm nemění a objem je přímo úměrný teplotě.
Výsledné diagramy
pV-diagram

VT-diagram





