Pravděpodobnost nalezení elektronu za Bohrovým poloměrem
Úloha číslo: 2018
Určete pravděpodobnost, že elektron v základním stavu atomu vodíku nalezneme ve větší vzdálenosti od jádra, než odpovídá poloměru jeho klasické dráhy, tj. Bohrovu poloměru.
Nápověda 1
Uvědomte si, co určuje Bohrův poloměr. Vyhledejte si jeho velikost.
Nápověda 2
Zamyslete se, jak se vypočítá pravděpodobnost nalezení elektronu v dané oblasti prostoru.
Nápověda 3
Zjistěte, jaký tvar má radiální část vlnové funkce popisující elektron v základním stavu atomu vodíku.
Řešení
Poloměr klasické dráhy, tzv. Bohrův poloměr \(a_B,\) udává poloměr kruhové dráhy, po které se pohybuje elektron v základním stavu v atomu vodíku, aniž by přitom vyzařoval energii.
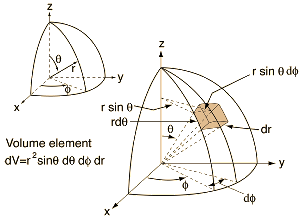
\(a_B=\frac{4\pi\varepsilon_0\hbar^2}{m_ee^2}\approx 0{,}052 917 7{\cdot} 10^{-9}\)mAtom vodíku je sféricky symetrický, proto bude výhodné úlohu řešit ve sférických souřadnicích \(r, \vartheta\) a \(\varphi\).
Pravděpodobnost \(P_{nl}\) nalezení elektronu v základním stavu atomu vodíku v závislosti na vzdálenosti \(r\) od jádra, konkrétně je-li vzdálenost \(r\) větší než Bohrův poloměr \(a_B\), je dána vztahem \[P_{nl}=\int_{a_B}^\infty{|R_{nl}(r)|^2r^2}\,\mathrm{d}r,\] kde \(n\) a \(l\) jsou kvantová čísla základního stavu atomu vodíku a \(R_{nl}(r)\) je radiální část vlnové funkce atomu vodíku v základním stavu. Odvození je uvedeno v Řešení nápovědy 2.
Základní stav atomu vodíku je určen kvantovými čísly \(n=1\), \(l=0\), \(m=0\) a protonovým číslem \(Z=1\). Radiální část \(R_{10}(r)\) vlnové funkce atomu vodíku v základním stavu popisuje funkce
\[R_{10}(r)=\left(\frac{Z}{a_B}\right)^{\frac{3}{2}}2\,\mathrm{e}^{-\frac{Zr}{a_B}}=\frac{2}{a_B^{3/2}}\,\mathrm{e}^{-\frac{r}{a_B}}.\]Nyní můžeme dosadit do \(P_{nl}\) a vypočítat pravděpodobnost \(P_{10}\), že elektron v základním stavu atomu vodíku nalezneme ve větší vzdálenosti od jádra, než odpovídá Bohrovu poloměru \(a_B\).
\[P_{10}=\int_{a_B}^\infty{|R_{10}(r)|^2r^2}\,\mathrm{d}r=\int_{a_B}^\infty{\left[\frac{2}{a_B^{3/2}}\,\mathrm{e}^{-\frac{r}{a_B}}\right]^2r^2}\,\mathrm{d}r=\]Funkci umocníme, konstanty vytkneme před integrál, dosadíme hodnotu integrálu (viz Výpočet integrálu) a upravíme.
\[=\int_{a_B}^\infty{\frac{4}{a_B^3}\,\mathrm{e}^{-\frac{2r}{a_B}}r^2}\,\mathrm{d}r=\frac{4}{a_B^3}\int_{a_B}^\infty{r^2\,\mathrm{e}^{-\frac{2r}{a_B}}}\,\mathrm{d}r=\frac{4}{a_B^3}\frac{5a_B^3}{4\,\mathrm{e}^2}=\frac{5}{\mathrm{e}^2}\doteq 0{,}68=68\,\text{%} \]Pravděpodobnost, že elektron v základním stavu atomu vodíku nalezneme ve větší vzdálenosti od jádra, než odpovídá Bohrovu poloměru, je 68 %.
Odpověď
Pravděpodobnost, že elektron v základním stavu atomu vodíku nalezneme ve větší vzdálenosti od jádra, než odpovídá Bohrovu poloměru, je 68 %.